上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
钙离子荧光探针Cal-590 钾盐
 |
货号 | 20519 | 存储条件 | 在零下15度以下保存, 避免光照 |
| 规格 | 1 mg | 价格 | 6564 | |
| Ex (nm) | 574 | Em (nm) | 588 | |
| 分子量 | 1123.03 | 溶剂 | Water | |
| 产品详细介绍 | ||||
简要概述
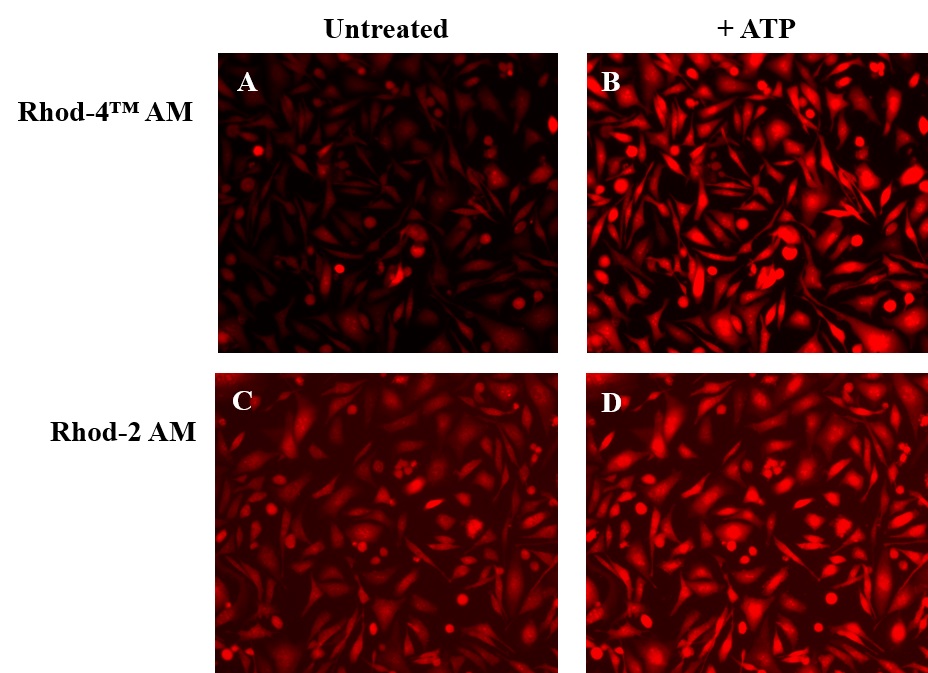
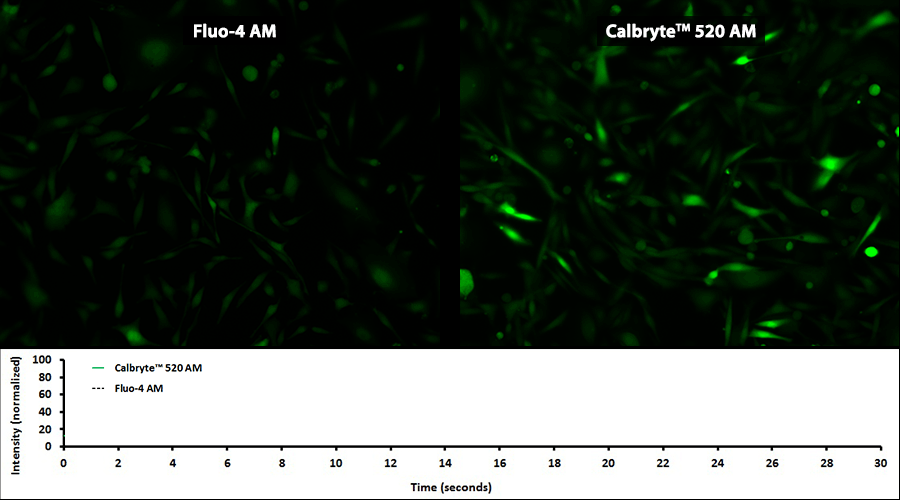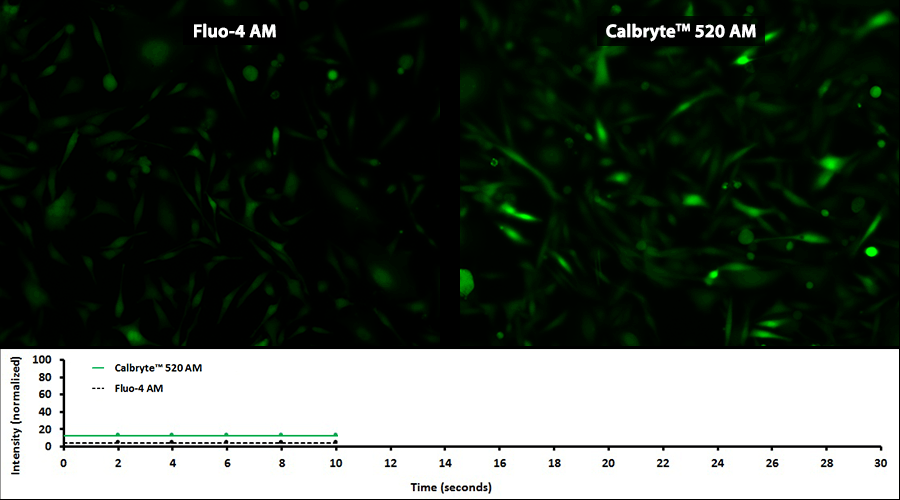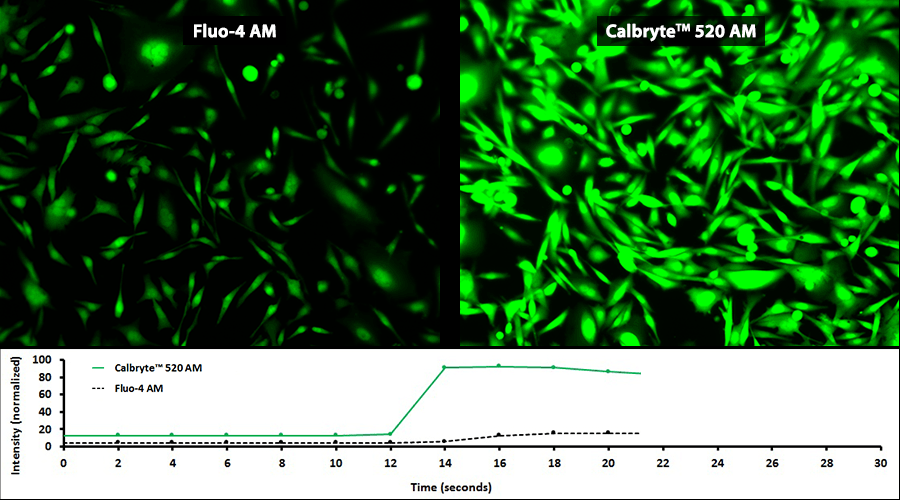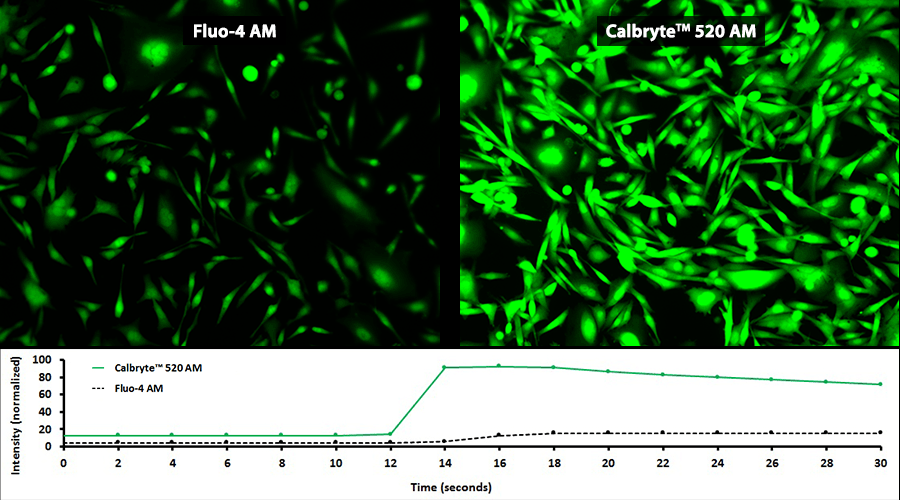
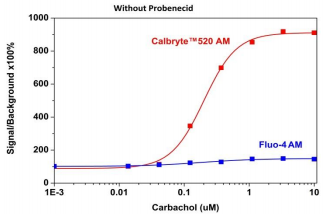
钙离子荧光探针Cal-590 钾盐是美国AAT Bioquest生产的钙离子荧光探针,钙的测量对于许多生物学研究至关重要。荧光探针显示结合钙的光谱响应,使研究人员能够通过荧光显微镜,流式细胞仪,荧光光谱和荧光酶标仪研究细胞内游离钙浓度的变化。 Rhod-2最常用于红色荧光钙指示剂中。然而,Rhod-2 AM在酯酶水解后仅在活细胞中发生中度荧光,并且具有非常小的细胞钙响应。 Cal-590 已被开发用于改善Rhod-2细胞负载和钙响应,同时保持Rhod-2的光谱波长,使其与TRITC /Cy3®过滤片组兼容。在CHO和HEK细胞中,Cal-590 AM具有比Rhod-2 AM更敏感的细胞钙响应。 Cal-590的光谱与FITC,AlexaFluor®488和GFP的光谱完全分离,使其成为用GFP细胞系或FITC / AlexaFluor®488标记抗体复合细胞内检测的理想钙探针。金畔生物是AAT Bioquest的中国代理商,为您提供最优质的钙离子荧光探针Cal-590 钾盐。
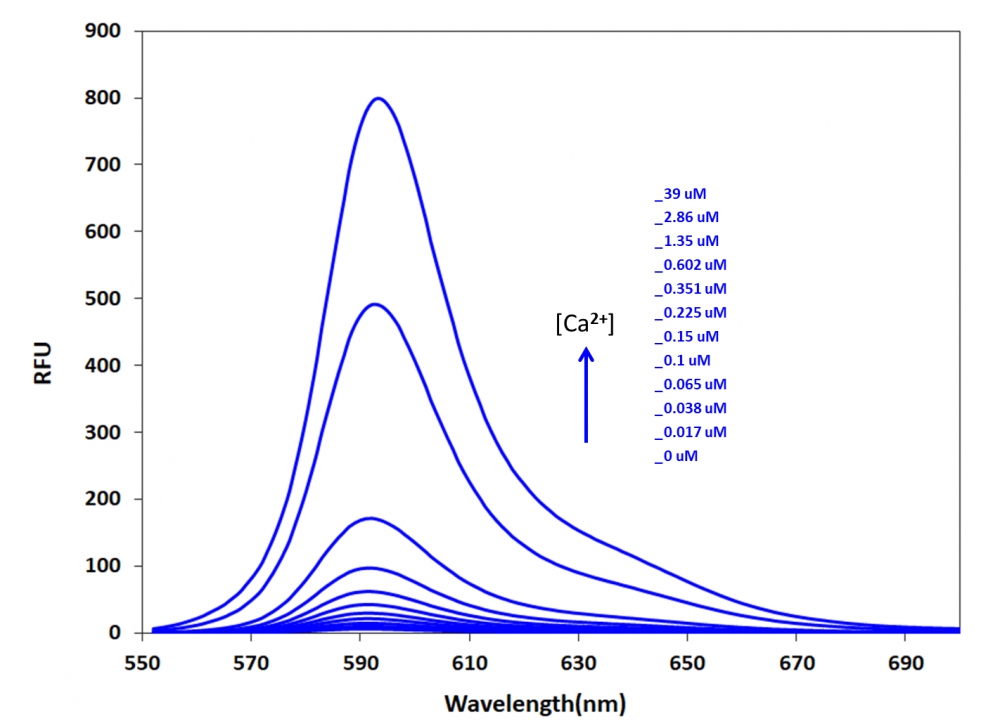
点击查看光谱
钙离子篇:时间轴式讲解应用于钙离子检测的探针
产品说明书
使用Cal-520 AM,Cal-570 AM或Cal-630 AM酯类
1.使用Cal-520 ,Cal-590 或Cal-630 AM酯:
AM酯是非极性酯,其易于穿过活细胞膜,并且通过活细胞内的细胞酯酶快速水解。AM酯广泛用于非侵入性地将各种极性荧光探针装载到活细胞中。但是,使用AM酯时必须小心,因为它们易于水解,特别是在溶液中。它们应在使用前重新配制成高质量的无水二甲基亚砜(DMSO)。DMSO储备溶液可以在-20℃下干燥储存并避光。在这些条件下,AM酯应稳定数月。以下是我们推荐的将Cal-520 AM,Cal-590 AM或Cal-630 AM酯加入活细胞的方案。该方案仅提供指南,实际应根据您的具体需求进行修改。
a)在高质量无水DMSO中制备2至5 mM Cal-520 AM,Cal-590 AM或Cal-630 AM酯的储备溶液。
b)在实验当天,将Cal-520 AM,Cal-590 AM或Cal-630 AM溶解在DMSO中或将等份的指示剂储备溶液解冻至室温。在Hanks和Hepes缓冲液(HHBS)或您选择的缓冲液(0.04%Pluronic®F-127)中制备10至20μM的染料工作溶液。细胞加载所需指示剂的确切浓度必须凭经验确定。
注意:非离子型洗涤剂Pluronic®F-127有时用于增加Cal-520 AM,Cal-590 AM或Cal-630 AM酯的水溶性。
c)如果您的细胞(如CHO细胞)含有有机阴离子转运蛋白,可将丙磺舒(1-2 mM)加入染料工作溶液中(最终浓度为0.5-1 mM)以减少渗漏去酯化指标。
d)将等体积的染料工作溶液(来自步骤b或c)加入细胞板中。
e)将染料加载板在细胞培养箱中孵育60至90分钟,然后在室温下将板孵育另外30分钟。
注意:孵育染料超过2小时可以为某些细胞系提供更好的信号强度。
f)用HHBS或您选择的缓冲液(含有阴离子转运蛋白抑制剂,如1mM丙磺舒,如果适用)替换染料工作溶液,以去除多余的探针。
g)在Ex / Em = 490 / 525nm(对于Cal-520 AM),540 / 5000nm(对于Cal-590 AM)或600 / 640nm(对于Cal-630 AM)进行实验。
2.测量细胞内钙响应:
为了确定溶液的游离钙浓度或单波长钙指示剂的Kd,使用以下等式:
[Ca]free = Kd[F ─ Fmin]/Fmax ─ F]
其中F是实验钙水平下指示剂的荧光,Fmin是不存在钙时的荧光,Fmax是钙饱和探针的荧光。
解离常数(Kd)是探针对钙的亲和力的量度。 与校准溶液相比,荧光指示剂的Ca结合和光谱性质在细胞环境中变化非常显着。 细胞内指标的原位反应校准通常产生显着高于体外测定的Kd值。 通过在离子载体如A-23187,4-溴A-23187和离子霉素存在下将加载的细胞暴露于受控的Ca2+缓冲液来进行原位校准。 或者,细胞透化剂如洋地黄皂苷或X-100可用于将指示剂暴露于细胞外培养基的受控Ca2+水平。
参考文献
Spatio-temporal modulation of light for stimulation and recording of neuronal activity
Authors: He Ma, Michael Lawrence Castanares, Vincent Daria
Journal: (2018): 1072306
A Critical Period for the Rapid Modification of Synaptic Properties at the VPm Relay Synapse
Authors: Libiao Pan, Junhua Yang, Qian Yang, Xiaomeng Wang, Liya Zhu, Yali Liu, Huifang Lou, Chou Xu, Ying Shen, Hao Wang
Journal: Frontiers in molecular neuroscience (2017)
Advances in Two-Photon Scanning and Scanless Microscopy Technologies for Functional Neural Circuit Imaging
Authors: Simon R Schultz, Caroline S Copeland, Amanda J Foust, Peter Quicke, Renaud Schuck
Journal: Proceedings of the IEEE (2017): 139–157
Bidirectional communication between sensory neurons and osteoblasts in an in vitro co-culture system
Authors: Daisuke Kodama, Takao Hirai, Hisataka Kondo, Kazunori Hamamura, Akifumi Togari
Journal: FEBS Letters (2017)
Ca 2+ signals initiate at immobile IP 3 receptors adjacent to ER-plasma membrane junctions
Authors: Nagendra Babu Thillaiappan, Alap P Chavda, Stephen C Tovey, David L Prole, Colin W Taylor
Journal: Nature Communications (2017): 1505
Calcium Imaging Across Large Areas of Intact Vascular Endothelium Reveals Stimulus-Specific Sensory Cells
Authors: Matthew D Lee, Calum Wilson, John G McCarron
Journal: The FASEB Journal (2017): 1005–8
Calcium transient assays for compound screening with human iPSC-derived cardiomyocytes: Evaluating new tools
Authors: Neil J Daily, Radleigh Santos, Joseph Vecchi, Pinar Kemanli, Tetsuro Wakatsuki
Journal: Journal of evolving stem cell research (2017): 1
Characterization of postsynaptic calcium signals in the pyramidal neurons of anterior cingulate cortex
Authors: Xu-Hui Li, Qian Song, Tao Chen, Min Zhuo
Journal: Molecular Pain (2017): 1744806917719847
Direct measurement of TRPV4 and PIEZO1 activity reveals multiple mechanotransduction pathways in chondrocytes
Authors: M Rocio Servin-Vences, Mirko Moroni, Gary R Lewin, Kate Poole
Journal: eLife (2017): e21074
Expression of the GluA2 subunit of glutamate receptors is required for the normal dendritic differentiation of cerebellar Purkinje cells
Authors: Masahiko Tanaka, Tomomi Senda, Naohide Hirashima
Journal: Neuroscience Letters (2017)
相关产品
| 产品名称 | 货号 |
| 钙离子荧光探针Cal-520 , AM | Cat#21130 |
| 钙离子荧光探针Fluo-8, AM | Cat#21080 |
| 新型钙离子荧光探针Calbryte 520, AM *细胞渗透性* | Cat#20650 |